Bài 3: Đốt cháy hoàn toàn 0,88 g X một hợp chất hữu cơ. Sản phẩm gồm 0,896 lít CO2 (đktc), và 0.72 g nước. Tỉ khối hơi của X so với không khí gần bằng 3,04. Xác định CTPT của X.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 0,88 gam hợp chất hữu cơ X (chứa C, H, O), thu được 8,96 lít khí CO2 ở đktc và 0,72 gam H2O. Tỉ khối hơi của X so với H2 là 44. Xác định công thức phân tử của X?
Bn check lại đề chứ mình nghĩ VCO2 = 0,896 (l)
\(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,72}{18}=0,04\left(mol\right)\)
Bảo toán C: nC(X) = 0,04 (mol)
Bảo toàn H: nH(X) = 0,04.2 = 0,08 (mol)
=> \(n_{O\left(X\right)}=\dfrac{0,88-0,04.12-0,08.1}{16}=0,02\left(mol\right)\)
=> nC : nH : nO = 0,04 : 0,08 : 0,02 = 2 : 4 : 1
=> CTHH: (C2H4O)n
Mà M = 44.2 = 88(g/mol)
=> n = 2
=> CTHH: C4H8O2
Đúng 2
Bình luận (0)
Hợp chất X chỉ chứa C,H,O. Đốt cháy hoàn toàn 1,76 gam chất X thu được 3,52 gam khí CO2 và 1,44gam nước . Tỉ khối hơi của X so với không khí xấp xỉ 3,04. Xác định CTPT của A . " Help me ................"
Xem chi tiết
nCO2 = 0,08 => nC = 0,08 mol
nH2O = 0,08 => nH = 0,08.2 = 0,16 mol
mX = mC + mH + mO => mO = mX - mC - mH = 1,76-0,08.12-0,16.1 =0,64 gam
nO= 0,64 : 16 = 0,04
Gọi công thức đơn giản nhất của X là CxHyOz => CTPT của X có dạng (CxHyOz )n
x:y:z = nC : nH : nO = 0,08 : 0,16 : 0,04 = 2:4:1
CTĐGN : C2H4O
Mx = 3,04.29 = 88 ==> (C2H4O)n = 88 => n =2
Vậy CTPT của X là C4H8O2
Đúng 0
Bình luận (0)
Hợp chất X chỉ chứa C,H,O. Đốt cháy hoàn toàn 1,76 gam chất X thu được 3,52 gam khí CO2 và 1,44gam nước . Tỉ khối hơi của X so với không khí xấp xỉ 3,04. Xác định CTPT của A . " Help me ................"
Xem chi tiết
Oxi hóa hoàn toàn 0.23gam hợp chất hữu cơ X thu được 0,224 lít khí Co2 (đktc) và 0,27gam nước A. Tính phần trăm các nguyên tố B. Cho tỉ khối hơi của X so với không khí 1,568. Xác định CTPT của X
\(n_{CO_2}=\dfrac{0.224}{22.4}=0.01\left(mol\right)\)
\(n_{H_2O}=\dfrac{0.27}{18}=0.015\left(mol\right)\)
\(n_O=\dfrac{0.23-0.01\cdot12-0.015\cdot2}{16}=0.005\left(mol\right)\)
\(\%C=\dfrac{0.01\cdot12}{0.23}\cdot100\%=52.17\%\)
\(\%H=\dfrac{0.015\cdot2}{0.23}\cdot100\%=13.04\%\)
\(\%O=100-52.17-13.04=34.79\%\)
\(n_C:n_H:n_O=0.01:0.03:0.005=2:6:1\)
CT đơn giản nhất : C2H6O
\(M_X=1.568\cdot29=46\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow46n=46\Rightarrow n=1\)
\(CT:C_2H_6O\)
Đúng 1
Bình luận (0)
nCO2= 0,01 (mol) -> nC=0,01(mol)
nH2O= 0,015(mol) -> nH=0,03(mol)
mX=mC+mH+mO
<=>0,23=0,1.12+0,03.1+mO
<=>mO=0,08
=>nO=0,005(mol)
Gọi CTTQ X: CxHyOz (x,y,z: nguyên, dương)
=>x:y:z=nC:nH:nO=0,01:0,03:0,005=2:6:1
=> CTĐGN C2H6O.
Mặt khác: M(X)= 1,568.29= 45,5 (thôi lấy tỉ khối 1,587 or 1,588 hợp lí hơn nha) (M(X) xấp xỉ 46 ~~~ )
=> (C2H6O)a=46
<=> 46a=46
<=>a=1
=>CTPT X : C2H6O
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,04 gam hợp chất hữu cơ X rồi cho sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy có 12 gam kết tủa và khối lượng bình tăng thêm 8,16 gam. Tỉ khối của X so với H2 bằng 38. Xác định CTPT của X
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CO_2} = n_{CaCO_3} = \dfrac{12}{100} = 0,12(mol)$
Ta có : $m_{bình\ tăng} = m_{CO_2} + m_{H_2O}$
$\Rightarrow m_{H_2O} = 8,16 - 0,12.44 = 2,88(gam)$
$\Rightarrow n_{H_2O} = 0,16(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,12(mol)$
$n_H = 2n_{H_2O} = 0,32(mol)$
$\Rightarrow m_O = m_X - m_C - m_H = 1,28(gam) \Rightarrow n_O = \dfrac{1,28}{16} = 0,08(mol)$
Ta có :
$n_C : n_H : n_O = 0,12 : 0,32 : 0,08 = 3 : 8 : 2$
Vậy CTPT của X : $(C_3H_8O_2)_n$
$M_X = 76n = M_{H_2}.38 = 76 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_2$
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 1.44g chất hữu cơ A thu đc 2.24 lít khí co2 dktc và 2.16g nước tỉ khối hơi của A so với hiddro bằng 36 xác định CTPT của Y
\(n_{CO_2}=0,1(mol);n_{H_2O}=0,12(mol)\)
Bảo toàn C và H: \(n_C=0,1(mol);n_H=0,24(mol)\)
\(\Rightarrow m_C=0,1.12=1,2(g);m_H=0,24.1=0,24(g)\\ \Rightarrow m_A=m_C+m_H\)
Do đó A chỉ chứa C và H
Gọi CTHH A là \((C_xH_y)_n\)
\(\Rightarrow M_A=36.2=72(g/mol)\\ x:y=0,1:0,24=5:12\\ \Rightarrow CTDGN_A:C_5H_{12}\\ \Rightarrow n.(12.5+12)=72\\ \Rightarrow n=1\)
Vậy \(CTHH_A:C_5H_12\)
Đúng 2
Bình luận (0)
Để đốt cháy hoàn toàn 2,85 g chất hữu cơ X phải dùng vừa hết 4,20 lít
O
2
(đktc). Sản phẩm cháy chỉ có
C
O
2
và
H
2
O
theo tỉ lệ 44 : 15 về khối lượng.1. Xác định công thức đơn giản nhất của chất X.2. Xác định công thức phân tử của X biết rằng tỉ khối hơi của X đối với
C
2
H
6...
Đọc tiếp
Để đốt cháy hoàn toàn 2,85 g chất hữu cơ X phải dùng vừa hết 4,20 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O theo tỉ lệ 44 : 15 về khối lượng.
1. Xác định công thức đơn giản nhất của chất X.
2. Xác định công thức phân tử của X biết rằng tỉ khối hơi của X đối với C 2 H 6 là 3,80.
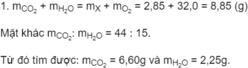
Khối lương C: 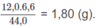
Khối lượng H: 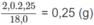
Khối lượng O: 2,85 - 1,80 - 0,25 = 0,80 (g).
Chất X có dạng CxHyOz
x : y : z = 0,150 : 0,25 : 0,050 = 3 : 5 : 1
Công thức đơn giản nhất của X là C 3 H 5 O .
2, M X = 3,80 x 30,0 = 114,0 (g/mol)
( C 3 H 5 O ) n = 114; 57n = 114 ⇒ n = 2.
Công thức phân tử C 6 H 10 O 2 .
Đúng 0
Bình luận (0)
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!Bài 1:Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.Bài 2:Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/...
Đọc tiếp
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
Đốt cháy hoàn toàn 3 (g) hợp chất hữu cơ X .thu được 4.4g CO2 và 1.8g H2O .biết tỉ khối của X so với H là 15 .xác định ctpt X
\(n_C = n_{CO_2} = \dfrac{4,4}{44} = 0,1(mol)\\ n_H = 2n_{H_2O} =2.\dfrac{1,8}{18} = 0,2(mol)\\ n_O = \dfrac{3-0,1.12-0,2}{16}=0,1(mol)\\ n_C : n_H : n_O = 0,1 : 0,2 : 0,1 = 1 : 2 : 1\\ CTPT : (CH_2O)_n\\ M_X = (12 + 2 + 16)n = 15M_{H_2} = 30\\ \Rightarrow n = 1\\ CTPT : CH_2O\)
Đúng 1
Bình luận (0)




















